Bagaimana Kesimpulan Yang Diperoleh Dobereiner Dalam Pengelompokan Spu
Lebih dikenal dengan Hukum Triade Dobereiner. Harga tetapan planck h yang diperoleh dari eksperimen efek fotolistrik oleh milikan 1917 sebesar 665 x 10-34 Js.
Berikut ini adalah tabel periodik Mendeleev.
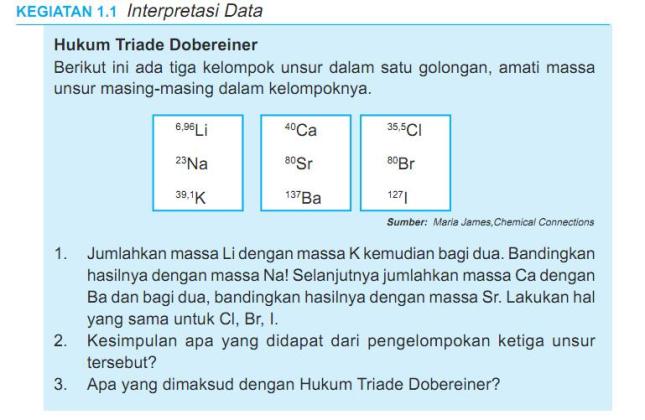
Bagaimana kesimpulan yang diperoleh dobereiner dalam pengelompokan spu. Advertisements Sejarah Perkembangan Sistem Periodik Unsur SPU Dan Penjelasannya Sistem periodik adalah suatu tabel berisi identitas unsur-unsur yang dikemas secara berkala dalam bentuk periode dan golongan berdasarkan kemiripan sifat-sifat unsurnya. Kegunaan utama He adalah sebagai cairan dalam krioskopi. Dobereiner meyimpulkan bahwa unsur-unsur dapat dikelompokan ke dalam kelompok-kelompok tiga unsur yang di sebut triade.
Akan tetapi Dobereiner belum berhasil menunjukkan cukup banyak triade sehingga aturan tersebut bermanfaat. Untuk pembahasan kali ini kami akan mengulas mengenai Sistem Periodik Unsur yang dimana dalam hal ini meliputi pengertian perkembangan konfigurasi periode golongan sifat gambar dan contoh nah agar dapat lebih memahami. Pengelompokan unsur tersebut berdasarka sifat kimianya.
Yaitu gas tanah logam dan non logam. Mereka diatur dalam urutan nomor atom dalam tujuh periode horisontal dengan lantanoid lantanum 57 hingga lutetium 71 dan actinoids aktinium 89 hingga lawrensium 103 ditunjukkan secara terpisah di. Tabel Sistem Periodik Mendeleev Kelemahan dan Kelebihan Unsur Kimia - Pada 1869 ilmuwan Rusia Dmitri Ivanovic Mendeleev mempublikasikan hasil penelitiannya mengenai pengelompokan unsur-unsur kimiaUnsur-unsur kimia dikelompokkan Mendeleev ke dalam 12 kelompok menurut kenaikan massa atom.
Berikut tabel periodik HD dan tabel periodik unsur lengkap dengan keterangannya. Harga ini cocok dengan harga yang diperoleh dari pengukuran radiasi 4. Kelemahan dari teori ini adalah pengelompokan unsur ini kurang efisien dengan adanya beberapa unsur lain dan tidak termasuk dalam kelompok triade padahal sifatnya sama dengan unsur dalam kelompok triade tersebut.
Sifat-sifat ini berubah secara berangsur-angsur dari atas ke bagian bawah golongan Li174 o C Na978 o C K637 o C Rb389 o C Cs285 o C 4. Dobereiner juga menemukan beberapa kelompok unsur lain seperti itu. Menurutnya anggota triade yang berada di tengah memiliki sifat sifat diantara kedua nggota triade lainnya dan memiliki massa atom relative yang merupakan rata rata dari unsur.
Newlands ahli kimia Inggris. Robert Boyle adalah orang pertama yang memberikan tentang definisi bahwa unsur adalah suatu zat yang tidak dapat lagi dibagi-bagi menjadi dua. Ilmuwan yang kali pertama mengelompokkan unsur kimia berdasarkan massa atom adalah Johann Dobereiner.
Unsur-unsur kimia di bagi menjadi empat kelompok. Pada 1789 Antoine Lavoiser mengelompokan 33 unsur kimia. Namun sayang Dobereiner tidak berhasil menunjukkan cukup banyak triade sehingga aturan tersebut tidak bermanfaat.
Neon digunakan untuk tabung sinar pemutusan muatan. Pengelompokan unsur dari Dobereiner ini kemudian disempurnakan oleh AR. Dobereiner juga menemukan beberapa kelompok unsur lain mempunyai gejala seperti itu.
Di dalam triade unsur ke-2 mempunyai sifat-sifat yang berada di antara unsur ke-1 dan ke-3 dan memiliki massa atom sama dengan massa rata-rata unsur ke-1 dan ke-3. Pada tahun 1829 Johan Wolfgan Dobereiner 1780 1849 membagi unsur unsur dalam kelompok kelompok yang terdiri dari tiga unsur yang di sebut Triade. Namun sayang Dobereiner tidak berhasil menunjukkan cukup banyak triade sehingga aturan tersebut bermanfaat.
Sejumlah besar elemen yang sama tidak dapat dikelompokkan ke dalam triade misalnya besi mangan nikel kobalt seng dan tembaga adalah elemen yang serupa tapi. Cara Dobereiner mengelompokkan unsur-unsur berbeda dengan cara Lavoisier. Dobereiner juga menemukan beberapa kelompok unsur lain mempunyai gejala seperti ituoleh karena itu Dobereiner mengambil kesimpulan bahwa unsur-unsur dapat dikelompokkan ke dalam kelompok-kelompok tiga unsur yang disebut triade.
Pada tahun 1846 Newlands mengemukakan teorinya yang dikenal dengan hukum Oktaf. Dobereiner mengelompokan setiap tiga unsur kimia yang sifatnya mirip dengan satu kelompok berdasarkan kenaikan berat atomnya. Unsur yang memiliki selisih satu oktaf akan menunjukkan kemiripan sifat.
Pada tahun 1807 ilmuan Jerman Johann wolfgang Dobereiner membuat pengelompokan unsur kimia. Pengelompokan unsur itu sendiri mengalami perkembangan dari pengelompokan unsur yang dilakukan oleh para ahli Arab dan Persia Dobereiner Newlands Mendeleyev Lothar Meyer Moseley hingga sistem periodik modern yang kita pakai hingga sekarang. Pengelompokan unsur mengalami perkembangan dari pengelompokan unsur yang dilakukan oleh para ahli Arab dan Persia Dobereiner Newlands Mendeleyev Lothar Meyer Moseley hingga sistem periodik modern yang kita pakai hingga sekarang.
Pada waktu itu baru sekitar 20 jenis unsur yang suda Tabel periodik unsur terdiri dari unsur-unsur kimia yang telah ditemukan atau dibuat. Pengelompokan unsur ini kurang efisien dengan adanya beberapa unsur lain dan tidak termasuk dalam kelompok triade padahal sifatnya sama dengan unsur dalam kelompok triade tersebut. Dalam teorinya Newlands menyusun unsur-unsur atas dasar kenaikan massa atom relatifnya.
Oleh karena itu Dobereiner mengambilan kesimpulan bahwa unsur-unsur dapat dikelompokan ke dalam kelompok- kelompok tiga unsur yang disbutnya triade. Argon dapat digunakan untuk menyediakan suatu lingkungan yang inert dalam peralatan laboratorium dalam pengelasan dalam lampu listrik yang diisi gas. Dobereiner mengelompokan setiap unsur kimia yang sifatnya mirip menjadi satu kelompok triad berdasarkan kenaikan berat atomnya.
Karena itu Dobereiner mengambil kesimpulan bahwa unsur-unsur dapat dikelompokkan ke dalam kelompok-kelompok tiga unsur yang disebutnya Triade. Na Ar Kr dan Xe diperoleh dengan fraksionasi udara cair. Pada 1829 ia mengelompokkan unsur-unsur kimia ke dalam suatu kelompok yang terdiri atas 3 unsur yang sifatnya sama TriadJika unsur-unsur dalam satu triade tersebut disusun menurut kenaikan massa atom-atomnya ternyata massa atom maupun sifat-sifat unsur yang kedua merupakan rata-rata dari.
SPEKTRUM ATOM DAN TEORI ATOM BHOR 41 Spektrum Atom Di samping mempunyai sifat listrik atom juga dapat menyerap atau memancarkan cahaya. Pengelompokan ini masih terlalu umum karena ternyata dalam kelompok unsur logam masih terdapat berbagai unsur yang memiliki sifat berbeda. Unsur-unsur yang termasuk dalam sub golongan yang sama pada tabel Mendeleev mempunyai sifat fisik dan kimia yang sama 3.
Tabel Periodik Unsur Kimia Sistem Sifat Dan Gambar Hd
Rencana Pelaksanaan Pembelajaran Rpp
Jelaskan Perkembangan Sistem Periodik Unsur Dari Yang Pertama Brainly Co Id
Sistem Periodik Unsur Kimia G10 Quipper Blog
Tabel Periodik Sistem Perkembangan Sifat Gambar Contoh
Posting Komentar untuk "Bagaimana Kesimpulan Yang Diperoleh Dobereiner Dalam Pengelompokan Spu"